- Heti Ajánlat
- Természet
- Történelem
- Kultúra
- Nyelvtudomány
- Életmód
- Technika
- Tudósok
- Közélet
- Diákoldal
- Olvasóink küldték
- Tanítástan
- Pszichológia
e-Learning
- Tudta-e?
- Egy átlagos villám 5-10 centiméter széles, és 3 kilométer hosszú!
40. szám - 2008. május 26.
VI. GENIUS konferencia és diákversenyE 260, ez meg mi?Ez az anyag az ecetsav. Már számos problémáról hallhattunk az ételadalékokkal kapcsolatban. Felmerült bennünk a kérdés, hogy a készítmények valóban a feltüntetett mennyiséget tartalmazzák-e az egyes anyagokból. Úgy döntöttünk, hogy utánajárunk.
|
|||||||||||||||||||||
|
DÖME Lili, TÓTH Ágnes, 3. osztály, Zentai Gimnázium Mentor: Máriás Ildikó Bevezető Már számos problémáról hallhattunk az ételadalékokkal kapcsolatban. Valóban vannak veszélyes ételadalékok, ezekről azonban többnyire tudunk is. Ez nem azt jelenti, hogy ilyenekkel nem találkozhatunk, csupán azt, hogy mérsékelt fogyasztásukkal az esetleges kellemetlen szövődményeket kiküszöbölhetjük. Nem nagy múltra tekintenek vissza az ételadalékok, ezért nem is lehetünk maradéktalanul tisztában azzal, milyen hatásaik lehetnek. Az E számok igen elterjedtek a köztudatban, találhatunk köztük igen veszélyeseket is, de vannak olyanok is, melyek teljesen ártalmatlanok számunkra, a mindennapi életben ismertek. Figyelmünket felkeltette ez a téma. Az egyik csomagoláson lettünk figyelmesek az E 260 jelölésre. Nem tudtuk, hogy mi lehet ez, így utánanéztünk. Azt találtuk, hogy ez az anyag az ecetsav. Ezután felmerült bennünk a kérdés, hogy a készítmények valóban a feltüntetett mennyiséget tartalmazzák-e az egyes anyagokból. Úgy döntöttünk, hogy utánajárunk. A titrálás A titrálás egy mennyiségi analitikai módszer, amelynél az ismert koncentrációjú reagens oldat segítségével meghatározhatjuk a vizsgált oldat hatóanyagtartalmát. A térfogatos elemzési módszerek alkalmazása közben a vizsgálandó anyag oldatához olyan ismert töménységű ún. mérőoldatot adunk, amely a meghatározandó vegyülettel gyorsan és teljesen végbemenő reakcióba lép. A mérőoldat térfogatából és koncentrációjából a reakcióegyenlet segítségével kiszámíthatjuk a vizsgált anyag mennyiségét. A meghatározás akkor pontos, ha a mérőoldatból annyit adagolunk, amennyi a reakció befejezéséhez éppen szükséges. A titrálás végpontjának meghatározására indikátort használnak, de történhet potenciometriás nyomonkövetéssel is. A leggyakrabban használt indikátorok a metilnarancs és a fenolftalein. A mérőoldat koncentrációját mol/dm3-ben adjuk meg, pontosságát a faktorral fejezzük ki. A faktor az a szám, amely megmutatja, hogy 1 ml mérőoldat hány ml pontos mérőoldatnak felel meg. Ha a F = 1, akkor pontos a mérőoldatunk; ha F > 1, akkor töményebb a mérőoldatunk; ha F < 1, akkor hígabb a mérőoldatunk. A titrálás alatt a titrált oldat összetétele folyamatosan változik. A meghatározandó anyag koncentrációja fokozatosan, majd a reakció befejeződésekor, a titrálás végpontjában ugrásszerűen csökken. A titrálás fajtái (a lejátszódó kémiai reakciók jellege szerint): Semlegesítéses: A ionok egyesülésén alapuló reakció. Savat lúgos, bázist pedig savas mérőoldattal titrálunk Oxidációs-redukciós: Elektronátmenettel járó reakció. Redukáló anyagot oxidáló, oxidáló anyagot pedig redukáló anyag mérőoldatával titrálunk. Csapadékos: Az elemzés során csapadékképződéssel járó reakció játszódik le. A vizsgálandó anyagot a lecsapó anyagból készült mérőoldattal titráljuk. Komplexometria: A mérőoldatot olyan vegyületből készítjük, amely a fémionokat komplex vegyület alakjában mennyiségileg meghatározható módon megköti. A titrálás módjai Közvetlen titrálás: A vizsgálandó anyag oldatát a mérőoldattal a reakció lejátszódásának végpontjáig titráljuk. Visszatitrálás: A mérőoldatot a vizsgálandó anyag oldatához feleslegben adjuk. A reakció lejátszódása után az el nem reagált mennyiséget alkalmas mérőoldattal meghatározzuk (visszatitráljuk). A hozzáadott és a visszatitrált mérőoldat különbsége adja a bemért anyagra fogyott mérőoldatot. Kiszorításos titrálás: A gyenge sav vagy gyenge bázis komponenst egy másik erősebb kiszorítja vegyületéből. A végpontban a só és a gyenge sav, vagy gyenge bázis van jelen a titrált oldatban. A végpontot a szabad sav ill. bázis kis feleslegének hozzáadása után a megfelelő indikátor színváltozásával határozzuk meg. Közvetett titrálás: Olyan ionok mérésére szolgáló módszer, amelyek a mérőoldat hatóanyagával nem reagálnak, vagy a keletkezett vegyület nem elég állandó. A mérendő iont vízben rosszul oldódó csapadékká alakítjuk. A lecsapásra használt reagens, vagy az ismert összetételű csapadék oldás utáni titrálására fogyott mérőoldat mennyiségéből számítással a mérendő anyag mennyisége meghatározható. Fordított titrálás: Ha a titrálás alatt a vizsgálandó anyag könnyen elbomlik más reakcióban, a vizsgálandó anyag oldatát töltjük a bürettába, és ezt adagoljuk a pontosan kimért mérőoldathoz. Az etánsav (ecetsav), CH3-COOH Az ecetsav híg vizes oldata már régóta ismert, mert hígabb szeszesitalok (bor, sör) a levegőn állva megecetesednek, azaz a bennük lévő alkohol ecetsavvá oxidálódik. Az ecetsav szúrós szagú, színtelen folyadék. Olvadáspontja 16,6 °C, ez alá hűlve kristályos, jégszerű tömeggé dermed, ezért a tömény ecetsavat szokás jégecetnek is nevezni. Az ecetsavmolekulák között is fellép hidrogénkötés, folyadékállapotban, sőt még gőzállapotban is – két molekula összekapcsolódásával – dimerek jönnek létre. Vízzel korlátlanul elegyedik, mert vízmolekulákkal is hidrogénkötést képez. Gyenge sav. Az ecetsav savmaradékionjának szabályos neve etanoátion, de a régi elnevezés, acetátion terjedt el. Lúgokkal sót képez. Negatív standardpotenciálú fémekkel (pl. Ca, Mg) hidrogént fejleszt. Az ecetsav – ellentétben a hangyasavval, de a többi zsírsavval megegyezően – nem mutat redukáló sajátosságokat, az oxidációval szemben igen ellenálló. Előállítása történhet alkoholból erjesztéssel. Ma már csak az ételek ízesítésére használatos ételecetet gyártják így, mert az eljárással csak híg ecetsav (kb. 10%-os) készíthető. A különböző gyümölcsborok szolgálnak a gyümölcsecetek előállítására. Az iparban ma nagy mennyiségben gyártják az acetaldehid katalitikus oxidációjával, vagy metanol katalitikus karbonilezésével. Az ipar nagy mennyiséget használ fel. Több szerves vegyület gyártásának kiindulási anyaga, használják oldószerként (főleg oxidációs reakciónál, mert az oxidációval szemben ellenálló), savanyú pácok készítésére, a gyógyszeriparban. A kísérlet menete A kísérletet különböző gyártók hat termékével végeztük: 1. Uborka – Medoprodukt, Tavankut 2. Uborka – Podravka, Bosznia és Hercegovina 3. Uborka – Vegafruit, Bosznia és Hercegovina 4. Paprika – Zora, Mohol 5. Fefferóni – Kopi Jukomerc, Kruševac 6. Gomba – Omega, Novo Selo, Vrnjačka Banja 0,1 mol/dm3 koncentrációjú NaOH oldatot használtunk, melynek faktora F=0,775 volt. Felhasznált eszközök: Pipetta Büretta Erlenmeyer-lombik Főzőpohár Üvegtölcsér Előkészítettük és megtisztítottuk az eszközöket a titráláshoz. Minden oldatból kimértünk 3-szor 10 cm3-t, melyeket előzőleg megszűrtünk és indikátorként fenolftalein oldatot adtunk hozzájuk. Ezután minden mintával 3-szor végeztük a titrálást. A titráláskor lejátszódó kémiai reakció: CH3COOH + NaOH → CH3COONa + H2O Ezután elvégeztük a megfelelő számításokat…
Befejezés A titrálás után megállapítottuk, hogy a moholi Zora paprikáját kivéve az összes felöntőlé a megfelelő tartományba beleeső savmennyiséget tartalmazza. A savtartalom mindegyik gyár esetében változó. A Podravka gyár uborkájának felöntőlevében találtuk a legkevesebb savat a többi uborkaléhez viszonyítva, ám ebben a termékben előfordult megpuhult uborka is, ami a kevesebb ecetsavtartalommal magyarázható. 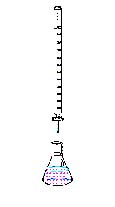 A titrálást ilyen eszközzel végeztük A titrálást ilyen eszközzel végeztükFelhasznált irodalom Balázs Lórántné dr. – J. Balázs Katalin: Kémia, ennyit kell(ene) tudnod Dr. Punger György: Analitikai kémiai laboratóriumi gyakorlatok (Titimetriás és gravimetriás módszerek) Fajka Valéria, Đorđević Ivan: Laboratóriumi kísérletek szerves kémiából Internet: www.freeweb.hu/hmika/Lexikon/Html/Titralas.htm www.kation.elte.hu/vegybank/tantov99/marosi/index.htm www.sci.u-szeged.hu/physchem/altkem/k002/gyak/titral.htm www.wikipedia.org/wiki/Titr%C3%A1l%C3%A1s |
Kapcsolódó cikkek
- Olvasóink ajánlata

